2023年12月18日,尹秀山教授团队又一最新研究成果“ARV-825 Showed Antitumor Activity Against BRD4-NUT Fusion Protein by Targeting the BRD4”于《Journal of Oncology》发表。
该项目主要研究了以BRD4为靶点,靶向BRD4-NUT融合蛋白,对中线癌(NC)有一定的治疗效果。中线癌(NC),又称NUT癌,具有强侵袭性、进展快、预后差、致死率极高等特点,即使采用积极的化疗,确诊患者的平均生存时间也不到1年(9.5个月)。目前现有的传统治疗手段整体效果欠佳,抑制剂等药物治疗仍存在耐药性及如何选择最合适的治疗组合局限。与传统的通过竞争性结合抑制作用的小分子不同,尹秀山教授团队首次利用泛素化蛋白水解技术(PROTAC)来靶向BRD4-NUT融合蛋白治疗中线癌,旨在为可能攻克中线癌提供有效的治疗策略。
中线癌是一种罕见的侵袭性鳞状细胞癌亚型,是由 NUTM1 基因重排引起,BRD4-NUTM1融合可在三分之二以上的NUT癌病例中被发现,预后较差。ARV-825 作为特异性靶向 BRD4 的 PROTAC小分子,具有较好的治疗潜力。该研究重点探讨了利用 PROTAC 化合物 ARV-825 作用于NC中的 BRD4-NUT 融合蛋白,以探究其抗癌效果。
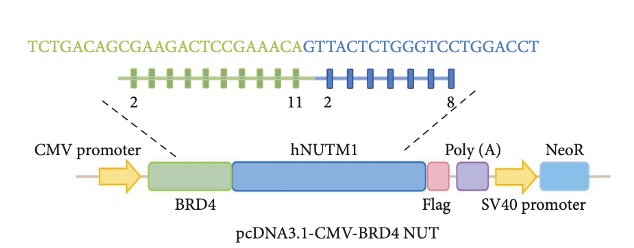
图一 CMV-BRD4-NUT载体构建方案
实验表明,BRD4-NUT 致病性融合基因的过表达可促进 3T3 细胞(小鼠胚胎成纤维细胞系)的增殖和迁移,并导致裸鼠皮下成瘤。进一步结合 RNA-seq 分析显示,BRD4-NUT 过表达后,表达显著上调的基因有E2F、TRAFs、Wnt、Gadd45g、Sox6 等,此外,small cell lung cancer, NF-kappa B signaling pathway, breast cancer 等通路明显富集,细胞周期由 G1 期进入 S 期,促进了细胞增殖和迁移,进一步激活抗凋亡信号,导致细胞异常生长,最终导致肿瘤发生。然而,研究发现,在加入靶向 BRD4 降解的 ARV-825 后,BRD4 蛋白表达水平发生快速且持续性的降解,有效地抑制了 BRD4-NUT 3T3 细胞的增殖和迁移。同时,通过细胞增殖活力及细胞迁移能力检测,发现 ARV-825成功抑制了 BRD4-NUT 3T3 癌细胞地增殖和迁移。总之,研究结果表明,BRD4-NUT 融合基因的过表达促进了3T3细胞的增殖和迁移,增强了3T3细胞的致瘤性,而靶向BRD4的PROTAC 小分子ARV-825对BRD4-NUT 3T3肿瘤显示了明显的抗肿瘤活性,如图二。这种利用 PROTAC 小分子的靶向疗法,可能是治疗具有 BRD4-NUT 融合事件遗传特征的中线癌的有效治疗策略。
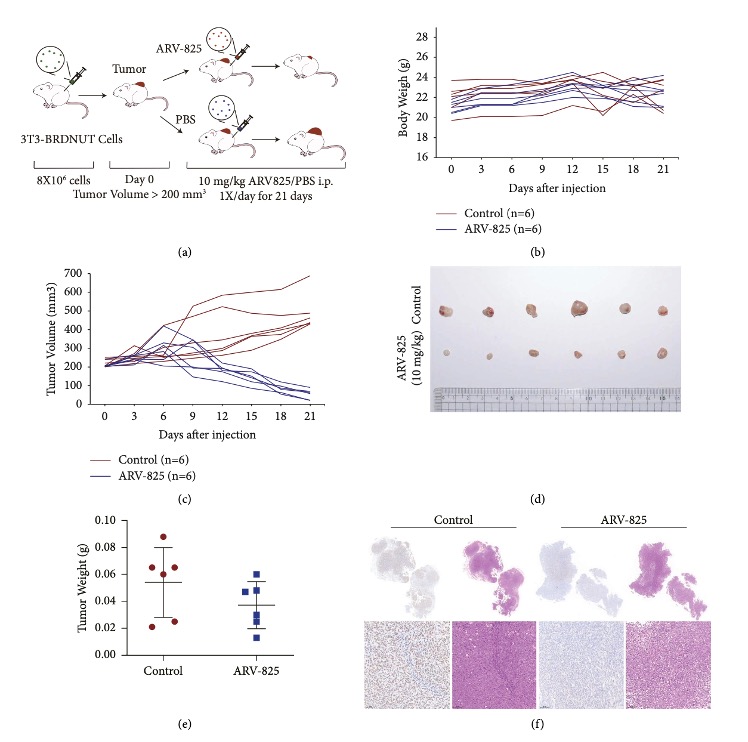
图二ARV-825在BRD4-NUT 3T3异种移植瘤模型中显示出抗肿瘤效果
总而言之,BRD4抑制剂ARV-825可能成为治疗具有BRD4-NUT融合事件基因特征的NUT癌的有效治疗策略。我们对细胞系的异位表达系统的研究极大地增加了我们对NUTM1融合蛋白所产生的分子改变的理解,为创造新的靶向药物提供了新思路,为个体化治疗提供了理论支持。PROTAC变革了小分子化药的成药方式,为靶向治疗开辟了新的途径,促进了中线癌治疗的进展。
该项目以沈阳化工大学为第一单位,合作单位有鲲石生物以及国家蛋白质科学中心(凤凰中心)。沈阳化工大学应用生物学研究所致力于开展创新科研项目研究,强调新思路,推动新技术,将高校基础技术学习研究与生产单位转化和科研机构技术创新双边接轨。